Ni水素2次電池
安全性の高さからHEVに採用
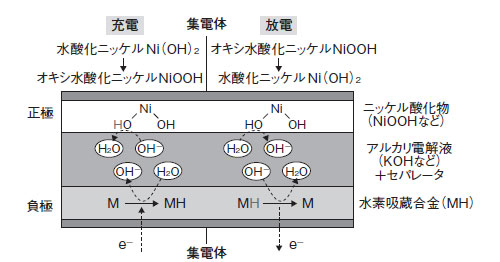
Ni水素2次電池は,正極に水酸化ニッケル(Ni(OH)2),負極に水素吸蔵合金,電解液として水酸化カリウム(KOH)水溶液を用いる(図5)。公称電圧は約1.2Vである。水素吸蔵合金は水素の吸蔵/放出プロセスが常温常圧で起こるように,水素を吸蔵しやすい金属と水素を吸蔵しにくい金属を適度に組み合わせて結合エネルギーを調整してある。水素吸蔵合金は,希土類元素とNiを基材としたものが多い。
Ni水素2次電池はLiイオン2次電池の登場により,国内出荷数量が大幅に減少した。ただし,安全性の高さには定評があり,ハイブリッド車には現在,Ni水素2次電池が使われている。
Liイオン2次電池
材料構成は多様
Liイオン(Li+)のロッキング・チェア機構†を使い,かつ金属Liを含まないのが,Liイオン2次電池である(図6)。負極に炭素材料,正極にコバルト(Co)系材料(LiCoO2,コバルト酸リチウム),電解質に有機溶媒とLi塩を用いたものが多い。公称電圧は3.7V前後である。負極と正極,電解質の各材料はLi+が移動でき,かつ電荷の授受により充放電可能であればよいので,非常に多くの構成を採り得る電池である。最近では安全性およびCoの価格高騰を背景に,Coに代わってマンガン(Mn)系や鉄(Fe)系の正極を用いたLiイオン2次電池の開発も,携帯機器や大電力の電気自動車向けに開発が進んでいる。
†ロッキング・チェア機構=充放電の際にゲスト・イオン(Liイオン2次電池ではLi+)が正負のホスト電極間を,揺りいすのように往復すること。
Liイオン2次電池では,正極活物質と負極活物質,電解液のすべての相でLiがLiイオン(Li+)として存在する。それにもかかわらず,炭素-LiCoO2系で約3.7Vもの起電力(φ+-φ-)が発生するのは,正極相と負極相のLi+の電気化学ポテンシャル(自由エネルギー)の差=(μ+-μ-)が大きいからである。電気化学ポテンシャルと電位差(φ+-φ-)の関係式は,
z×F×(φ+-φ-)=(μ+-μ-)
z:イオン価(Liの場合は1),F:ファラデー定数
で表される。
Liイオン2次電池を形状で分類すると円筒型,角型,ラミネート型がある。円筒型は低コストで,充放電時でも外形寸法が安定している。ただし多数のセルを組み合わせた場合にはすき間ができ,体積効率が悪くなる。角型は充電時に膨張するので,設計時に外形寸法に余裕を設けておく必要がある。ラミネート型は,円筒型や角型で使う金属缶の代わりにラミネート・フィルムを用いたものである。角型同様に充放電サイクルによって厚さが変化する。
ハイブリッド車用には高い出力特性を持ったラミネート型セルが開発されている(図7)1)。特徴は大きく二つある。(1)従来の円筒型に比べて半分以下の体積で,パワー密度を約1.5倍にできる,(2)薄型セル構造のため冷却効果が大幅に向上する上,薄型モジュール化が可能で車両の床下へ搭載した場合,フロアを低くフラットにすることが可能,ということである。


















































